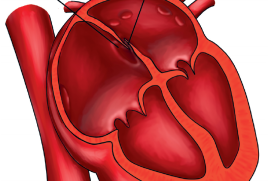
Quelles sont les bonnes indications de la fermeture percutanée dans la CIA ?
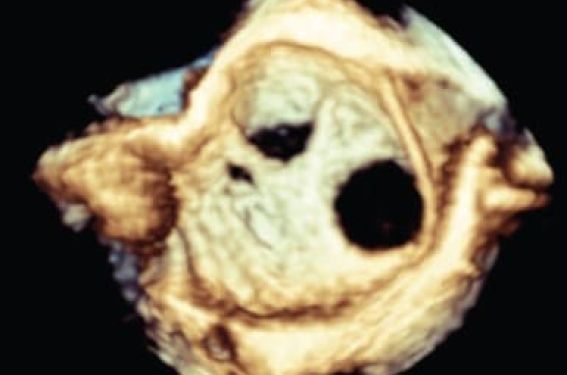
La fermeture par cathétérisme interventionnelle est maintenant proposée en première intention pour le traitement des communications interauriculaires ostium secundum(1). L’évolution du matériel disponible, le développement de techniques modifiées pour la mise en place de prothèse dans les cas complexes, font dire à certains que les contre-indications à la fermeture des CIA par voie percutanée sont maintenant « difficiles à trouver », et qu’il faut « fermer les petites CIA, car elles sont petites, et les grandes, car elles sont grandes »(2) !
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante