Publié le
Lecture 10 mins
Les bonnes indications de l'IRM cardiaque
J. GAROT, service d'IRM cardiovasculaire, Institut cardiovasculaire Paris Sud, Hôpital privé Jacques Cartier, Massy
Ce paragraphe non exhaustif a pour objectif de donner une vision synthétique des bonnes indications de l’IRM cardiaque. Pour chaque pathologie, un zoom est effectué sur les principaux signes ainsi que sur la valeur particulière et souvent ajoutée de l’IRM. L’ensemble est illustré par des exemples typiques.
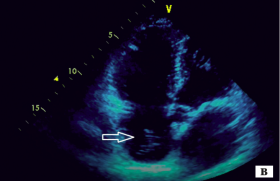
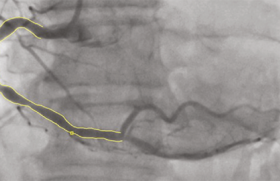
Cardiomyopathies ischémiques Situation chronique : l’IRM permet l’analyse quantifiée précise des paramètres de fonction VG, la recherche d’une ischémie myocardique provoquée par une IRM de stress (ciné-IRM sous forte dose de dobutamine-atropine, ou imagerie de perfusion sous dipyridamole ou...
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante