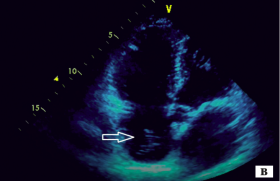
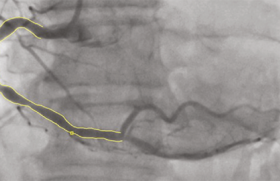
Angioscanner coronaire : une nouvelle prise en charge de la maladie coronaire ?
Pourquoi l’angioscanner coronaire va modifier nos habitudes dans le diagnostic et la prise en charge de l’angor d’effort ?
L’opportunité de visualiser de manière non invasive la lumière artérielle coronaire, par simple injection intraveineuse d’un produit de contraste iodé, est le rationnel fondamental de l’intérêt que manifeste aujourd’hui la communauté médicale à l’égard du scanner cardiaque ou plus exactement de l’angioscanner coronaire. Toute la question est de savoir quelle place réserver à cette nouvelle technique dans la stratégie diagnostique de la maladie coronaire.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante