Publié le
Lecture 16 mins
Doppler tissulaire myocardique et cardiopathies
G. DERUMEAUX, hôpital Louis Pradel, Bron et G. HABIB, CHU la Timone, Marseille
Les cardiomyopathies ischémiques et les cardiomyopathies hypertrophiques
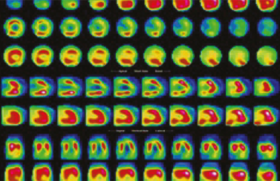
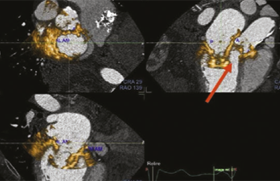
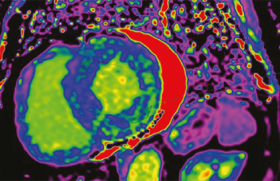
Cardiomyopathies ischémiques L’analyse de la fonction myocardique régionale est précieuse pour, d’une part, évaluer l’existence d’anomalies dans le cadre des syndromes ischémiques, d’autre part, reconnaître l’état fonctionnel du myocarde après reperfusion afin de pouvoir prédire une éventuelle...
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page précédente
- Page 2
- Page suivante