Angioplastie coronaire assistée par robot : mythe ou réalité ?
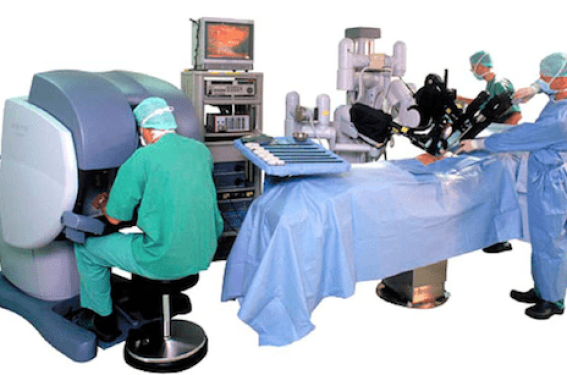
La robotique occupe une place croissante en médecine. Son application a débuté en chirurgie dans les années 2000. L’urologie a rapidement fait bénéficier les patients de ce progrès technologique, notamment lors des prostatectomies chez les patients atteints de cancer(1). Aujourd’hui, presque toutes les disciplines chirurgicales utilisent la robotique en pratique courante comme la gynécologie, la chirurgie thoracique et cardiaque, la chirurgie digestive ou encore ORL. En 2011, la robotique a fait également son apparition en angioplastie coronaire dans le but de réduire, d’une part, l’exposition aux rayons X des opérateurs et, d’autre part, les lésions musculosquelettiques induites par le port d’un tablier plombé.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante