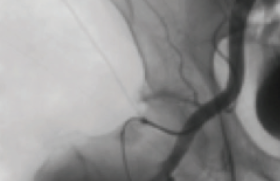
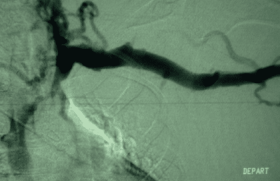
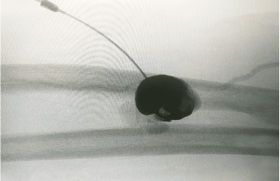
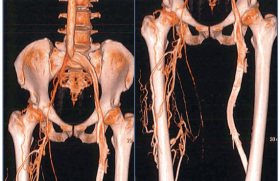
Lithotripsie intravasculaire et lésions artérielles obstructives calcifiées des membres inférieurs
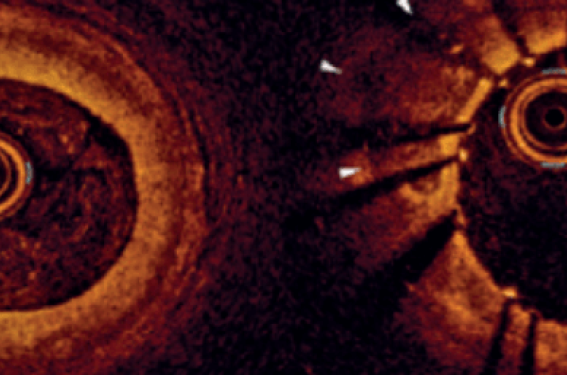
Une proportion considérable de lésions obstructives des artères des membres inférieurs traitées par intervention instrumentale endovasculaire présente des calcifications sévères connues pour laisser présager des taux de réussite procéduraux plus faibles, une augmentation des effets indésirables peropératoires et des résultats cliniques défavorables par rapport aux plaques non calcifiantes. La lithotripsie intravasculaire (LIV) par ondes de choc est une technique récente innovante issue de la thérapie établie pour les calculs rénaux et urétéraux. Elle repose sur l’utilisation d’un cathéter muni d’un ballon à basse pression dans lequel sont transmises des ondes acoustiques permettant de fractionner les plaques calcifiées in situ ce qui améliore la compliance de la lésion et facilite l’implantation et l’expansion symétrique de stent en diminuant le risque de dissection occlusive et de microembolisation distale.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante