Publié le
Lecture 12 mins
De petites artères, mais un grand enjeu de santé publique
Éric JOUVENT, Service de neurologie, CHU Lariboisière, Paris
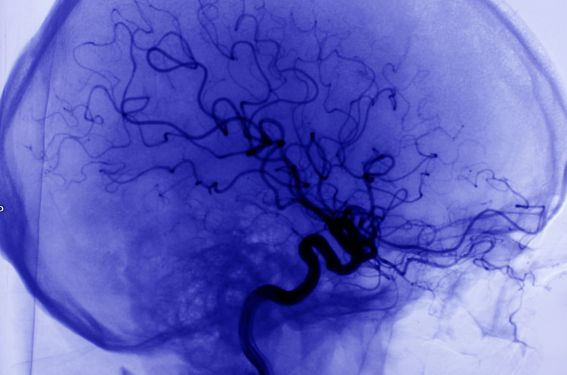
CADASIL est une maladie génétique des petites artères cérébrales à l’origine d’AVC parfois multiples. Le point sur une pathologie à laquelle il importe de penser devant certains tableaux cliniques.
Les AVC représentent une cause majeure de handicap et de troubles cognitifs dans les pays industrialisés (1). Ils peuvent être liés à la diminution sous un seuil critique de l’apport en oxygène (AVC ischémique) ou être secondaires à la rupture d’un vaisseau (AVC hémorragique). Parmi les AVC...
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
Pagination
- Page 1
- Page suivante



